水は物質を溶かす
”水”の最大の特徴とは何でしょう。いろいろあげられると思いますが、1つだけ取り上げるとすれば物質を溶かす性質ではないでしょうか。私たちが普段から利用している”水”は純粋な水だけであることはほとんどありません。多くの場合、何かの物質が溶け込んでいます。例えば私たちの体内をめぐる”水”には様々な物質が溶け込み、生命の維持に必要な物質の運搬·貯蔵、不要な物質の排泄などの働きをしています。
なぜ”水”は物質を溶かすことができるのでしょう?そもそも物質が溶ける現象とは具体的にどのような状態なのでしょうか。今回は水について(3)で書いた電気的にかたよっている性質をもつ”水”がその特徴を大いに発揮する、物質を溶かす性質について考えていきます。
溶ける現象とは?
物質が何かに溶ける状態は物質の分子レベルで考えると、溶ける物質と溶かす物質がなじむ状態ということができます。「なじむ」と言ってもピンとこないかもしれませんので、物質の最小単位である分子で考えてみます。物質は分子レベルで何かにくっつこうとする力が常に働いており(分子間力など)、単一物質の固体や液体では同じ物質同士がくっついています。この時、ある物質の分子が異なる分子とくっつき、それが連続すると物質が溶けた状態となります。
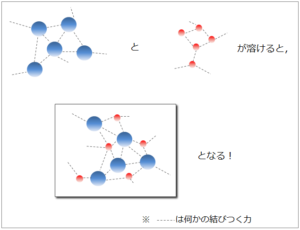
ところで似たような状態として混合気体がありますが、この場合は異なる分子が混ざり合ってはいますが(例えば大気)、互いにくっつこうとする力はほとんど働かないので溶けているとは表現しません。
”水”に溶けるとは?
”水”の場合はどうでしょう。水について(3)のとおり水分子同士は水素結合しています。水素結合は+と-の電気的な結合なので、もしこの結合付近に+の物質や-の物質が存在すれば水素結合に入り込むことができます。この状態が連続すると水に溶けた状態となります。
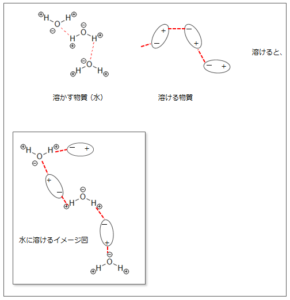
少し別の見方をしてみます。水が電気的にかたよっている分子であることを化学式で表すと、
H2O ⇄ H+ + OH–
とあらわすことができます。これは水分子(H2O)の状態とイオン状態(H+、OH–)が行ったり来たりしている状態です。水分子が電気的にかたよっているといっても、常に同じ大きさのかたより方をするわけではなく、かたより方が大きくなったり、小さくなったりと揺らいでいます。したがってこの式は水分子の状態をうまく表現していると思います。
この化学式の状態で考えると、H+と-の物質、OH–と+の物質とがくっつき、連続した状態が溶けた状態となります。
いずれの見方にしても+と-の結合が”水”に溶ける重要なポイントとなります。したがって、”水”に溶ける物質とは+と-にかたよっている物質ということができます。そして、多くの物質が多少なりとも+と-にかたよっているので、微量な場合を含めば、ほとんどの物質が”水”に溶けることになります。これが”水”に多くのものが溶ける原理です。ところで、種類にもよりますが一般的に”油と水は分離する”ので「油は”水”に溶けないじゃん!」と思うかもしれません。しかしその実体は、溶ける量がわずかであるため、溶けきれなかった油が集まりくっついて”水”と分離した状態となっているのです。
物質を溶かした”水”、すなわち物質が溶け込んだ”水”(水溶液)は溶けこんだ物質によっていろいろな性質をしめすようになります。次回はそのあたりのお話にしようと思います。

